骨髓间充质干细胞可治疗酒精性肝病
[本文为疾病百科知识,仅供阅读] 发布日期:2019-09-06 阅读:1,675我国是肝病大国,近年来,随着预防接种普及、抗病毒药物的应用,病毒性肝炎发病率逐年减少,但随着我国经济社会的发展、生活习惯的改变,酒精性肝病的发病率在我国却有升高趋势。长期大量饮酒是酒精性肝病发生的一项重要原因,酒精性肝病(Alcoholic liver disease; ALD)是一系列的疾病的总称,包括单纯性脂肪肝、脂肪性肝炎、肝硬化。现今临床上对其缺乏确实有效的改善方法。干细胞是一类具有无限自我更新与增殖能力并能产生至少一种高度分化子代细胞的细胞,有研究显示它对酒精性肝病具有显着的疗效。
一、酒精性肝病发病机制及病理生理特点
酒精性肝病(ALD)是一系列的疾病的总称,包括单纯性脂肪肝、脂肪性肝炎、肝硬化。长期大量饮酒是发病的一个重要原因,其中 90%-100%可发展为酒精性脂肪肝,10%-35%发展为酒精性肝炎,8%-20%发展为酒精性肝硬化。此外,过量饮酒的负面影响还包括促进其他类型慢性肝病如非酒精性脂肪性肝炎、乙型肝炎和丙型肝炎的进展,加速肝纤维化的进展。酒精性肝病的发病机制十分复杂,可能与酒精及其毒性代谢产物对肝内各种细胞的毒性作用、诱导的活性氧(ROS)以及过表达的炎症级联反应等多种因素之间相关作用有关。

酒精性脂肪肝是酒精性肝病的早期表现,超过 90%的重度饮酒者都有该症状,其病理特征是肝细胞内小泡和大泡性脂肪堆积,炎症反应轻,无肝纤维化。
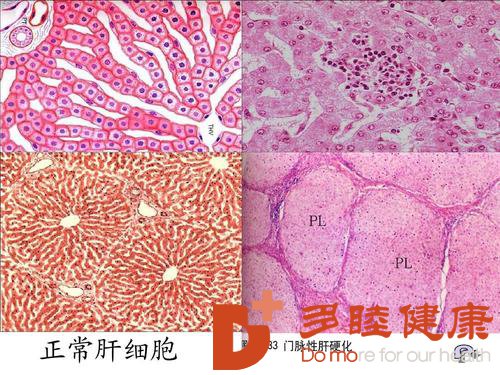
此阶段是无症状的,戒酒以后此过程是完全可逆的[6]。饮酒可增加肝细胞中NADH/NAD+比值,破坏线粒体脂肪酸的 β-氧化,从而导致脂肪变性的进展[7]。通过上调胆固醇调节元件结合蛋白-1c 和下调过氧化物酶体增殖物激活受体 α 的表达 [8-9],增加脂肪酸、甘油三酯合成。ALD 进展期的主要病理特征是脂肪变性、多形核白细胞的炎性浸润和肝细胞的损伤。当出现严重的炎症和肝细胞损伤时被称为脂肪性肝炎,这时伴随而来的是较高的死亡率[10]。酒精性脂肪性肝炎的病理学特征包括炎症和坏死,主要发生在肝细胞小叶中心区,同时出现的肝细胞气球样变,导致肝血窦受压和门静脉高压。细胞外基质(ECM)(特别是Ⅰ型胶原)主要由位于肝细胞和肝窦之间的 Disse 间隙活化的肝星状细胞(HSCs)产生。中性粒细胞,受损的肝细胞以及活化的肝巨噬细胞激活通过各种促纤维化因子,如转化生长因子(TGF-β),肿瘤坏死因子(TNF-α),活性氧激活肝星状细胞。此外,活性氧簇抑制金属蛋白酶功能,上调基质金属蛋白酶组织抑制剂-1 的表达,从而造成更大量的胶原堆积。酒精性肝硬化是酒精性肝病的终末阶段,该时期的病理特征是肝脏结构变形,纤维间隔形成,以及瘢痕结节、再生结节,从而导致肝功能的丧失。
酒精性脂肪性肝炎的发病机制是多因素参与的,非常复杂的。在肝脏中酒精的代谢主要是在细胞质的乙醇脱氢酶,过氧化氢酶体里的过氧化物酶,微粒体的细胞色素 P450 酶共同作用下代谢为初级产物乙醛[15]。乙醛对肝细胞有很强的毒性,因为它与蛋白质和脱氧核糖核酸结合形成加合物进而促使谷胱甘肽耗竭,脂质过氧化和线粒体损伤[16]。此外,这些加合物作为抗原可以激活免疫反应,导致淋巴细胞趋化至肝脏。乙醛在肝脏中分解产生的乙酸释放进入血液循环系统,在心脏、骨骼肌肉、脑通过三羧酸循环进一步被代谢为 CO2。虽然乙酸没有直接的肝脏毒性,但认为它可通过刺激单核巨噬细胞释放的促炎细胞因子来加重酒精性脂肪性肝炎患者的体内炎症反应程度。
过度饮酒也可导致结肠菌群生态系统发生变化和肠道的通透性增加,进而导致细菌产物(如脂多糖内毒素)易位进入门静脉循环。肝脏巨噬细胞中的脂多糖通过 Toll 样受体 4 激活 My D88 依赖的信号通路,发生氧化应激和炎性细胞因子(如 TNF-α)释放,导致肝细胞损伤。
和其他肝脏疾病一样,酒精性肝硬化患者也会出现肝功能失代偿症状(腹水、食管静脉曲张破裂出血、肝性脑病)和发生肝细胞癌的风险。虽然 ALD最重要的危险因素是酒精摄入的绝对量,但只有约 35%的重度饮酒者会发展成为 ALD,这表明其他因素也参与影响了宿主对疾病的易感性。这些因素包括性别、饮食、吸烟、肥胖、饮酒的模式,非性别遗传因素]。

二、酒精性肝病的改善
1、常规改善
虽然酒精性肝硬化对经济和健康问题影响深远,但过去的数十年中关于ALD 的患者的改善有了少些进展,而 ALD 的改善一直没有重大进展 [10]。虽然营养和支持改善是非常重要的,但戒酒仍然是各个阶段的 ALD 患者可靠的改善方法。然而,仅仅戒酒仍不足完全控制失代偿期肝病,如肝硬化或重症酒精性肝炎。
糖皮质激素是改善酒精性肝炎的最早药物之一。尽管这种疗法已经被普遍认识和使用,但关于其真正疗效的争议仍然存在。考虑到 TNF-α 参与了 ALD的发病过程,对于 TNF-α 拮抗剂改善酒精性肝炎也进行了相关的研究。虽然最初的研究是有应用希望的,但更进一步的大量临床试验表明这些药物能增加感染和死亡风险。此外,还有许多关于 ALD 改善药物被研究,但其功效有限。
晚期酒精性肝硬化最有效的改善方法是肝移植,但是由于供体缺乏、手术并发症、免疫抑制、排斥反应以及高额的医疗费用限制了其在临床实用性和应用价值[33],此外对于大多数患者来说没有机会接受肝移植改善。直到现在没有其他的改善要优于类固醇。因此,找到新的替代疗法是非常必要的。最近几年提出的新的细胞移植方法(如移植不同来源的细胞)能给解决肝脏供体缺乏问题。
2、肝细胞再生的细胞改善
众所周知,肝脏具有很高的再生能力。在正常情况下肝体积的恢复主要是通过剩余的成熟肝细胞的增殖。另一方面,在病理条件下肝细胞的增殖受到抑制,肝脏祖细胞(卵圆细胞)则增殖和分化为肝细胞或胆管上皮细胞。慢性酒精摄入和持续的炎症已被证明能抑制受损肝细胞 DNA 合成。这种肝细胞增殖的受损是由酒精代谢产生的活性氧的氧化所造成的。此外,乙醇还可以抑制肝祖细胞向功能成熟肝细胞的早期分化。
三、骨髓间充质干细胞改善肝脏疾病机制
目前对于骨髓间充质干细胞移植后肝脏疾病得到缓解存在多种机制,包括骨髓间充质干细胞向肝细胞分化,免疫调节,抑制肝纤维化的发展,对肝细胞的保护作用,恢复肝细胞的增殖能力。因此骨髓间充质干细胞移植是改善酒精性肝病的一个非常有希望的方法。
1、分化为实质细胞
骨髓间充质干细胞可以通过生殖细胞屏障,分化为非中胚层以外的细胞(如肝细胞和神经元)。重点的是要注意间充质干细胞来源的肝细胞不但需要表达在成熟肝细胞上所具有的基因种类,而且基因表达水平也要接近正常肝细胞的表达量。
2、调控炎症反应
持续的炎症反应引起的肝损伤通常伴随着 T 细胞、B 细胞和单核细胞肝脏浸润。因此在炎症方面,骨髓间充质干细胞可以通过免疫调节和免疫抑制特性在急性和慢性肝脏疾病中起积极作用。 骨髓间充质干细胞可以调节先天性和适应性免疫细胞的活性。在体外实验发现骨髓间充质干细胞抑制前体细胞分化为树突状细胞。因此,骨髓间充质干细胞可以间接限制 NK、T 淋巴细胞活性和细胞毒性扩大。无论是在体外和体内,骨髓间充质干细胞都可以下调促炎症分子的表达分泌抗炎因子、促使免疫应答模式向保护型 Th2细胞免疫模式转变,使在其中激活的 T 细胞不能增殖并且发生凋亡,建立免疫耐受的微环境。骨髓间充质干细胞可以促进调节性 T 细胞的出现,从而诱导抗原特异性耐受。
干细胞改善是改善酒精性肝病一个新兴的改善方法。骨髓间充质干细胞是一个极具潜力的改善策略,因为其已被证明能够诱导受损的肝组织再生,并且在临床前或临床研究中并没有发现有明显不良反应的证据。由于酒精性肝病进展中的病理变化与间充质干细胞改善效果相关的细胞和分子机制之间有一定的联系,我们相信,骨髓间充质干细胞移植是能控制酒精性肝病进展的一个很有前途的改善策略。
本文链接地址:http://www.domo-kenkou.com/gxbzs/2094.html










