干细胞治疗心血管疾病现状
[本文为疾病百科知识,仅供阅读] 发布日期:2019-10-15 阅读:1,749心脏仅有有限的自我再生能力,因此,心肌受损或梗死后的改善需要外源性的细胞加以修复,目前研究最多的是干细胞改善。干细胞按来源不同分为胚胎于细胞和成体干细胞。干细胞移植后,心脏的功能有改善,但其具体机制是移植细胞自身作用,还是细胞旁分泌作用或其他,各研究提供的证据不一。
心脏组织中的干细胞
心脏虽有有限的自我再生能力,但大多数心肌细胞在受损后会被巨噬细胞吞噬而代之以瘢痕组织,其受损部位周围的心肌收缩功能很差;如心肌梗死(简称心梗)或其他长期严重的心肌损伤的患者当中, 65%会在5年内出现心力衰竭(简称心衰);这是由于成体心脏缺乏心肌祖细胞而致再生能力差所导致的。受损的心肌之所以不能通过细胞再生获得修复,其原因是心肌细胞不能分裂增殖,心肌中也没有存留的类似干细胞的多潜能细胞。然而,wu等…近几年来研究发现,在人类及小鼠的心脏内存在着数量极少的表达干细胞标志的细胞群,这些被表达的干细胞标志蛋白有Kit、干细胞抗原1(SCAl)以及多抗药性蛋白l(MDRI)。但也有人认为这群存在于心脏组织中表达Kit的细胞是微量残留在组织中的骨髓细胞,不是真正的心肌细胞,而是异位的骨髓细胞瞳l。此外,近期研究发现成人心脏活组织样本中表达Kit的细胞同时也是表达肥大细胞的标志,而胚胎时期心脏祖细胞的决定性标志——心脏转录因子NKX2-5及isletl(Isll)并未表达,因此认为这些细胞不是心脏祖细胞。

细胞改善心脏病
目前成体干细胞已经应用于临床改善,广为人知的是对肿瘤病人进行的干细胞移植。随着干细胞研究的深入开展,对心脏病尤其是缺血性心脏病进行干细胞移植,成为许多科学家关注的课题。Orlic等"1分别将成体干细胞注入心梗小鼠模型的梗塞灶旁健康的左室心肌组织中,其中一组小鼠被注射细胞因子将成体干细胞动员至梗死部位,两组结果均被证实成体干细胞能在梗塞部位形成新生的心肌细胞及冠状血管。千细胞移植后新生的心肌细胞如果具有收缩功能,让这些心肌细胞取代受损的心肌,那将有望防止或纠正心梗后产生的心衰;此外,新生的心肌细胞除需具有收缩功能,更为重要的是,它们还必须与宿主心肌细胞收缩同步。曾有报道将骨骼肌细胞分化而来的肌细胞/成肌祖细胞移植到啮齿类心梗动物模型中,改善了左室射血分数等指标,但因为新生的心肌细胞无法与原有的心肌细胞收缩同步,可能导致心律失常,从而无法用于临床。骨骼肌成肌细胞及生肌祖细胞除了能分化为骨骼肌细胞外,最新的研究表明,它还可以表达缝隙连接蛋白CX43【6J,以改善梗死灶与周围正常组织间的电交联;这虽可促进心肌细胞产生正常电生理作用,但由于成体心肌细胞植入后存活率不如胎儿肌细胞高,对植入的心肌细胞电生理作用的正常发挥可能带来不利影响。
成体干细胞来源的心肌细胞移植改善
干细胞可塑性的观点提出不久,Orlic掣引就报道了例骨髓细胞转分化形成心肌细胞。在这项研究中小鼠骨髓细胞被绿色荧光蛋白标记后移植入心梗野生小鼠的心脏后,可以在小鼠心脏组织中检测出绿色荧光蛋白的表达,而野生型小鼠受损的心功能也有所恢复。由于心梗及心衰病人的临床改善需要,这项技术已迅速应用于临床改善,目前已进入临床试验阶段¨…。但最近的随机对照研究在经过长期随访之后显示,改善并不像原先的非随机非对照研究那样有效。那些注射了不同分化类型细胞的病人,左室射血分数并未提高或仅提高不到5%¨h“1;尽管如此,至少在干细胞改善后前4~6个月内,一些长效参数如梗死后重建及运动功能等的确有所改善,改善对那些患有大面积梗死灶的心梗患者尤为有效。
在对早期研究的重复性试验中人们发现,虽然将骨髓细胞注入心梗小鼠后可以表达出类似心肌细胞标志的骨髓细胞,但这并未证明骨髓细胞一定发生了转分化,同时研究者却发现有极少部分的骨髓细胞可以与心肌细胞融合并同时表达骨髓及心肌两种细胞标志。在对啮齿类及体型较大的哺乳动物的一些实验研究表明,在稳定移植物形成之前即出现了新生血管形成、缺血心肌复苏等变化,这些证据均显示细胞移植改善后心功能的改善可能跟移植细胞的旁分泌作用对缺血心肌的保护作用有关,而未必是由于新生的心肌细胞取代了受损细胞的结果。有人认为多能干细胞移植有可能在体内形成一些无用的细胞,Breitbach等¨纠报道在移植改善后的心肌组织中发现了骨及软骨系细胞,当然这也有可能是因为注射时使心肌损伤后钙化所致。
干细胞移植入组织后并不一定都有生理功能。脐带血、脂肪细胞或外周血等多种组织来源的各种类型的细胞,无论是被直接注入心脏或经静脉注人,其游走到病灶的特征均与骨髓细胞相似。有观点提出移植改善后的心功能改善可能是由于植入细胞的旁分泌作用所致¨“。成体祖细胞进行移植后会释放出炎性介质及血管生长因子,这些现象也不是稳定移植物产生的作用。还有人报道胸腺素一p4可以影响存在于-C,夕1-膜上内生上皮祖细胞群的移行及血管化。
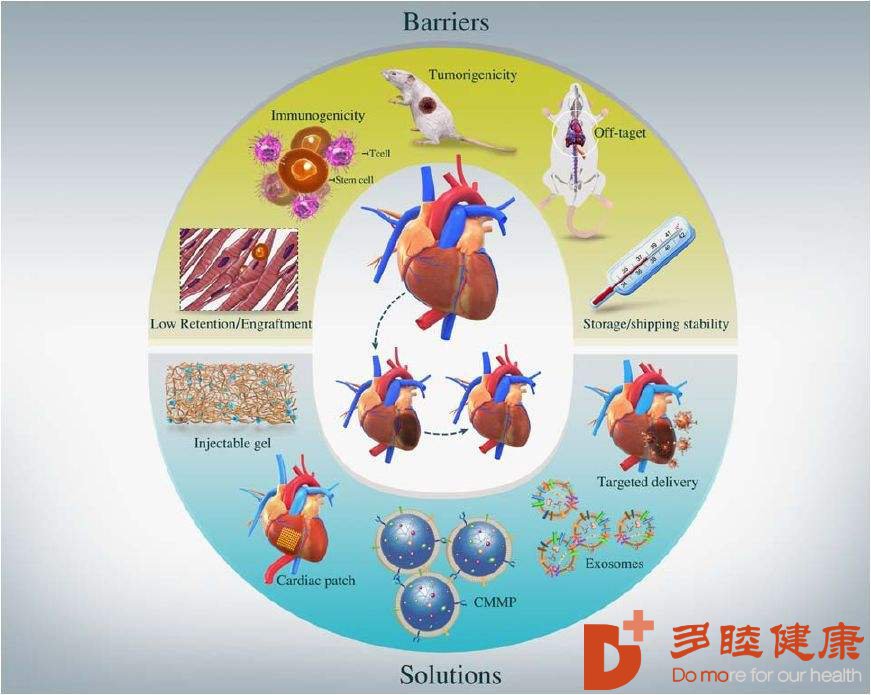
胚胎干细胞来源的心肌细胞移植改善
有研究者对房室传导阻滞的豚鼠进行人胚胎千细胞移植改善,发现人胚胎干细胞有发挥生理起搏点功效的潜能¨…。目前只有人胚胎干细胞分化来的心肌细胞能在梗死灶形成肉眼可见的移植物。与非心肌细胞移植对照组相比,移植人胚胎干细胞分化的心肌细胞的小鼠在4周后心脏功能就得到了改善;人胚胎干细胞分化的非心肌细胞移植组与仅注入细胞培养液的对照组相比,心功能也有所改善,且随着植入后时间的延长,非心肌细胞移植组的心功能的改善效果似乎也在提高;不过,心肌细胞组植入效果明显优于非心肌细胞组。
对心脏进行的其他类型分化细胞移植治
移植细胞与宿主细胞的融合需要构建血管来提供氧气和养分。报道将人胚胎干细胞诱导分化成内皮细胞,他们利用这些细胞所具有的血小板内皮细胞粘附分子1的抗体特异性,把分化的内皮细胞分离出来,然后注射到小鼠皮下,注射部位事先已放置可生物降解的支架,这些内皮细胞形成了血管样结构。其他研究者也利用人类胚胎干细胞分化的平滑肌细胞及内皮细胞进行了移植,同样也发现人源性血管与宿主循环系统建立了联系,这种联系甚至一直持续到移植后5个月。
现有的血管网相连。虽然利用不同来源细胞移植的临床研究正在积极开展,但是仍有很多问题未得到解决。除了探讨细胞移植对心脏的改善效果外,在不同情况下(如急性心梗或慢性心衰)选择何种细胞类型、细胞改善的最佳时限以及有效分化的方法等还有待进一步明确。Moelker等Ⅲ1认为冠状动脉内注射细胞悬液,需要细胞准确定位到病灶,同时还有发生微小梗
血管内皮细胞对修复心肌起了重要作用。首先,新生血管可以保护梗死灶周围的心肌。其次,植入的心肌细胞自身需要额外的血液供应,尤其是当移植物与宿主管脉间有纤维相隔时。移植所产生的新生血管内皮细胞可能有助于移植物与现有的血管网相连。虽然利用不同来源细胞移植的临床研究正在积极开展,但是仍有很多问题未得到解决。除了探讨细胞移植对心脏的改善效果外,在不同情况下(如急性心梗或慢性心衰)选择何种细胞类型、细胞改善的最佳时限以及有效分化的方法等还有待进一步明确。
推荐阅读:日本干细胞:仝小林治疗糖尿病经验
本文链接地址:http://www.domo-kenkou.com/gxbzs/2219.html










