干细胞“再生技术”一个潜在的创伤治疗手段
[本文为疾病百科知识,仅供阅读] 发布日期:2019-10-21 阅读:1,938什么是干细胞?干细胞在急诊创伤改善中到底扮演一个什么样的角色?
干细胞是一种多功能细胞,能够再生人体的各种组织,因此在创伤改善中有一定的临床潜力,特别是在骨折愈合、软骨愈合及创伤后炎症等方面。

1干细胞的生物学
身体里的再生细胞可以根据能力来进行分类,其中再生能力最强是全能型的胚泡细胞,然后是多功能干细胞、祖细胞和前体细胞(如下图所示),这些细胞具有内在的再生能力,当然这里面也有与创伤相关的特殊干细胞。干细胞是未分化的细胞,从三个原始生殖层(内胚层、中胚层和外胚层)发展而来,具有自我更新和分化为各类成熟细胞的能力。干细胞是在全身的某个局部微环境中被发现的,在这个环境中干细胞处于未分化的休眠状态。在干细胞和邻近细胞之间存在多种分子机制控制着其分化和自我保护。这里主要介绍与创伤修复相关性的4种细胞:间质干细胞(MSC),造血干细胞(HSC),脐带干细胞(MSCs),和内皮祖细胞(EPC)。其中MSC和HSC大部分主要存在于骨髓内,EPC位于内皮细胞。值得注意的是,目前有新技术可以将收获的体细胞转化为诱导多能干细胞(iPSC)并获得潜在的再生能力。
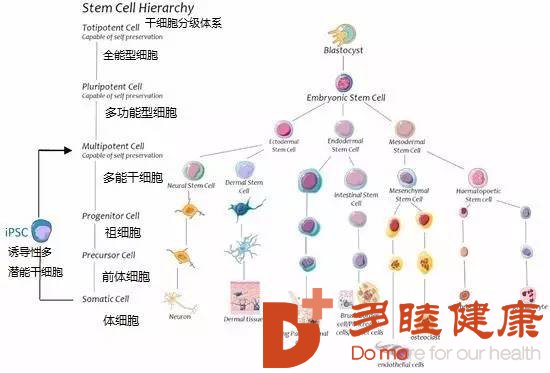
间质干细胞(MSC)是一种多功能的干细胞,可以在中胚层内分化成任何非造血细胞,如成骨细胞、软骨细胞、脂肪细胞和骨髓细胞。它们的特征是细胞表面携带标志物CD105、CD73和CD90。MSC可以在多个部位采集,包括肌肉、脂肪组织、骨髓和脐带中,现有技术可以在体外进行筛选、培养和增殖以供在机体移植时使用。MSC是临床改善中最多的一类干细胞,骨髓间质干细胞由于缺乏MHC II类分子和协同刺激分子使得它们免疫原性削弱,与多功能胚胎干细胞相比它们也不会导致畸胎瘤的形成,这些性质使得它们在自体和异体的临床应用中更有吸引力。
干细胞(HSC)能够分化成为粒细胞或淋巴细胞,这些细胞的特征是表面携带标志物CD34、CD45、CD133和Thy1,它们能从骨髓及外周血中获得,可在恶性肿瘤如白血病细胞、淋巴瘤和骨髓衰竭等同种异体移植中应用。
脐带干细胞(ADSC)由胎盘组织中获得,与骨髓来源的间质干细胞功能相似,这些细胞的特征是表面携带标志物CD90、CD73和CD44。
内皮祖细胞(EPC)具有血管生成的潜力,它们存在于外周循环中,表面携带标志物CD34,Flk-1和Tie-2。

2创伤对干细胞的影响
创伤导致组织结构性破坏,使组织灌注受损,并诱发炎症反应。干细胞对创伤的生理反应包括从它们的休眠状态中苏醒,从它们的原始居住场所中动员并向受伤的部位迁移,最后分化产生改善所需的特定细胞。此外,病理性的炎性反应不仅会导致干细胞的功能失调,同时会使干细胞的数量减少,最终将导致组织再生失败或其他不良预后。
在创伤后MSC与HSC的迁移已被许多趋化作用阐明。其中一种信号途径就是下图所示的基质衍生因子1/特异性趋化因子受体4(SDF-1/CXCR4)轴。这条信号轴解释了干细胞在局部停留及向受伤部位迁移的过程。CXCR4是骨髓间质干细胞的一种受体,它能结合SDF-1。SDF-1是一种由骨髓内皮细胞和基质细胞表达的蛋白质,继受伤后,SDF-1在组织损伤的部位产生,其浓度高于骨髓,从而促进骨髓中MSC向受伤部位转移。SDF-1的表达受缺氧诱导因子-1(HIF-1)和一氧化氮(NO)调控。在正常生理情况下,骨髓中的SDF-1浓度有利于保留骨髓间质干细胞。这在动物骨折和心肌损伤模型中已被证实, CXCR4 受体的上调也使得间质干细胞向SDF-1迁移得到进一步加强。
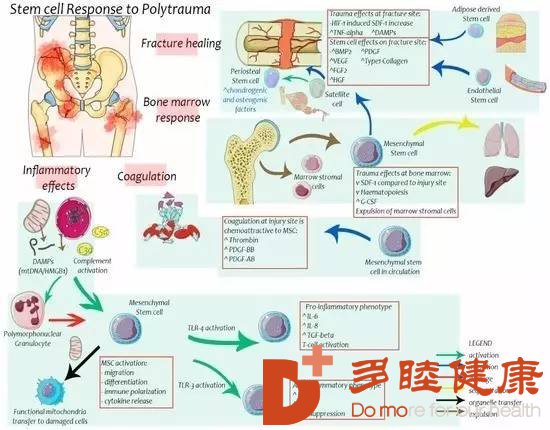
3干细胞在创伤愈合中的作用
骨折会引起骨髓内MSC的增生,骨折后会引起在骨髓和骨膜内的常驻干细胞迁移至损伤部位。在骨折部位需要有一定数量的干细胞进行修复,同时骨萎缩也被证实与骨折部位缺乏MSC有关。
充足的血供是干细胞迁移并存活的必要条件。Atesok, K等发现在小鼠骨折后进行纯化的EPC注射,有利于血管增生及更快的骨折愈合:在骨折部位EPC的血管生成效应与增加的亲血管生成因子hVEGF、hFGF2和hHGF 44的局部水平相关;同时还发现MSC的迁移与增加的小鼠骨痂体积和强度有关联。MSC约在EPC使用后第14天出现在骨折部位。这些改善效果与MSC迁移后局部BMP-21(骨形态生成蛋白)的表达有关。
干细胞已被证明能对机械刺激产生反应。体外改善已经证实了干细胞对以下刺激有反应,如牵拉、压迫、剪切、震荡、超声波等。在拉伸、压迫和超声波等刺激下,干细胞可表现出成骨分化。相反地,Dai等人发现,对小鼠的MSC进行反重力作用的改善可抑制其成骨分化。有改善表明在体外改善时,低强度脉冲超声波可促进MSC的成骨转化。
4干细胞在软骨愈合中的作用
干细胞的功能与关节软骨损伤的恢复以及创伤后骨关节炎有关。在损伤的发生后,关节软骨中的MSC会分化成纤维细胞,而不是软骨细胞。创伤时关节组织纤维化的情况更少,由此表明创伤可引起干细胞分化的变化,并与创伤后骨性关节炎息息相关。
通过干细胞在关节内注射能改善创伤引起的软骨缺损。半月板组织再生增加,伴有骨关节炎患者的疼痛评分得到改善,且没有出现严重的不良反应。
使用MSC的改善方法有望能够改善骨关节炎和创伤后的软骨缺损。目前改善的重点是确定最佳的MSC来源、如何在植入前进行体外改造及更安全地使用。关于骨关节炎改善的已有多篇文献得出肯定的结论。
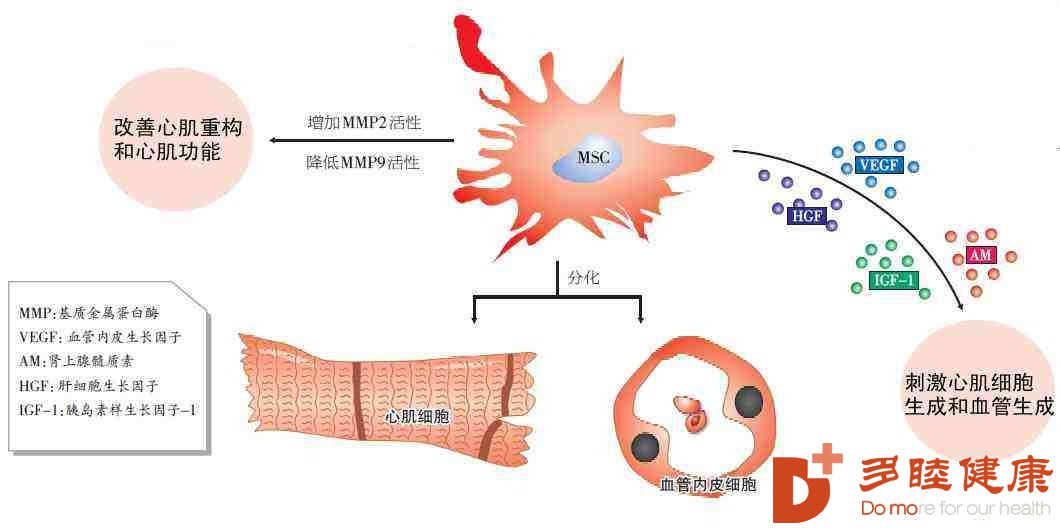
5干细胞在血管生成中的作用
对于创伤修复来说,恢复良好的血供是改善的关键。创伤可导致急性和迟发性的毛细血管损伤,包括直接伤害、血管闭塞或因外科手术改善创伤时所造成的医源性损伤。在受伤后,干细胞对血管生成有直接和间接的影响。一些改善表明,EPC迁移到受伤的部位后直接参与了新生血管的形成。其他的改善也已经证实EPC通过生长因子、细胞因子的调节促进新生血管生成。MSC和ADSC也有促进血管生成的类似作用。这些干细胞的血管生成功能最终有助于改善骨折的愈合、毛细血管再生、伤口的康复及减少炎症并发症。
6干细胞在外伤后炎症反应中的应用
干细胞具有免疫调节功能,MSC可以转化为促炎症和抗炎细胞,它主要依赖于在创伤后炎症反应中分泌的介质如Toll样受体(TLR)。TLR是一种表面受体,它能结合病原体分子和损伤相关模式分子 (一类由创伤后细胞破坏释放的内源性产物,包括线粒体DNA(mtDNA),高机动性的编组框-1蛋白质和S100蛋白质等,具有激活免疫细胞的能力),在调控炎症反应中起着重要的作用。
创伤后引起的中性粒细胞和巨噬细胞激活会对干细胞造成损伤。在机体受伤后,中性粒细胞和干细胞一起迁移到受伤的部位,但它们迁移到创伤部位的时间点不同。中性粒细胞被激活后会释放活性氧,无意中损害了周围的细胞包括干细胞。如果损伤足够严重,中性粒细胞的激活状态持续存在(尤其是在细胞凋亡之后),那么干细胞就可能会被破坏。
严重的创伤后会导致骨髓衰竭,创伤后高炎症反应状态和G-CSF(粒细胞集落刺激因子)浓度升高将导致骨髓干细胞造血功能受损,并容易引发感染。在动物改善中发现通过MSC改善能逆转骨髓损伤
干细胞在改善骨折愈合方面,从文献检索到多项临床案列、以及大量的动物改善和基础改善。干细胞疗法在通过组织再生和免疫调节改善创伤后,对改善患者预后有很大的帮助,是改善创伤最有效安全的疗法。
推荐阅读:日本干细胞|避免错误,早日走出糖尿病阴影
本文链接地址:http://www.domo-kenkou.com/gxbzs/2241.html










