糖尿病导致的皮肤愈合治疗方法还要等多久?
[本文为疾病百科知识,仅供阅读] 发布日期:2019-09-16 阅读:1,734皮肤伤口愈合是一个复杂的生物整合过程, 包括细胞外矩阵分子、可溶性介质及细胞因子等向伤口处的聚集、多种细胞的增殖及迁移、胞外基质沉积及血管新生等。然而, 在一些慢性疾病中, 这些有序的整合过程被破坏。其中, 糖尿病是影响皮肤伤口愈合的慢性疾病之一。
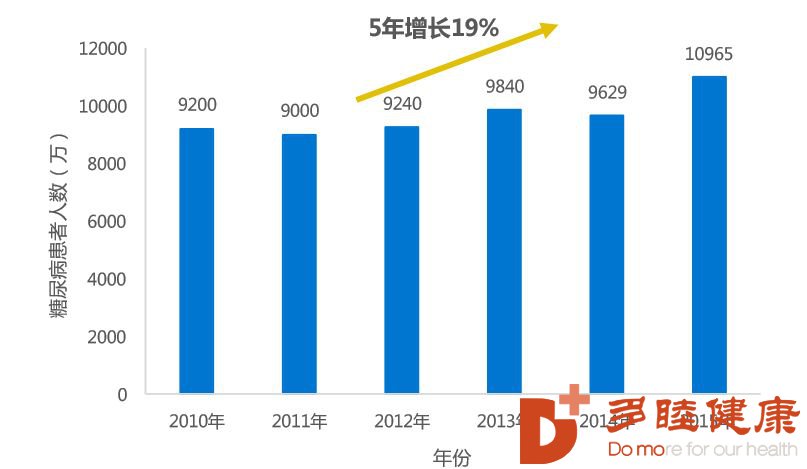
根据 2013 年国际糖尿病联盟公布的数据, 年龄在 20~79 岁的成人中糖尿病的患病率为 8.3%且患者人数已达 3.82 亿, 估计到 2035年将有近 5.92 亿人患糖尿病。2013 年, 1/4 的糖尿病患者为中国人, 中国糖尿病人数已超过 1 亿, 位列。11%中国成年人为糖尿病患者, 其中 50%处于糖尿病前期。
糖尿病患者常伴有难愈性足部溃疡, 即使接受的改善, 愈合率也仅为 50%, 且复发率高, 并最终导致截肢等严重后果。同时, 糖尿病患者极易发生血管病变, 如血管生成障碍、内源性再生反应受阻, 血管内多种生长因子水平降低、胶原合成减少及蛋白水解酶增加, 血管和组织生成障碍等。
糖尿病患者伤口愈合障碍严重影响人们的日常生活, 有效地预防和改善糖尿病伤口愈合障碍具有重要的临床意义。目前, 临床上常规改善方法包括清创和局部伤口用药等。近年来, 临床上出现了一些新的改善方法, 如电刺激、生长因子和负压改善等, 均难以改善糖尿病伤口愈合情况。
随着分子生物学的发展, 干细胞 (stem cells, SCs) 和 microRNA 以及再生医学研究已成为临床转化医学方面最有前景的研究领域。干细胞是一类具有自我复制和更新能力的多潜能细胞。按照发育阶段, 干细胞可分为胚胎干细胞 (embryonic stem cells, ESCs) 和成体干细胞 (adult stem cells, ASCs)。其中成体干细胞包括间充质干细胞 (mesenchymal stem cells, MSCs)、内皮祖细胞 (endothelial progenitor cells, EPCs)、脂肪干细胞 (adipose-derived stem cells, ADSCs) 及造血干细胞 (hemopoietic stem cell, HSCs) 等。一定条件下, 成体干细胞可分化成多种功能细胞。干细胞的这种多向潜能性使其在组织修复中发挥重要作用。近年来, 干细胞对糖尿病伤口改善作用的研究取得突破性的进展, 有望成为新的改善手段并应用于临床。
1、干细胞移植改善糖尿病伤口愈合的机制
干细胞是一类未成熟细胞, 可以通过添加特异的诱导因子或抑制分化因子, 将干细胞诱导分化成各种不同类型的细胞。通过干细胞技术和组织工程学技术, 可诱导干细胞定向分化, 使其分化为特定的细胞以替代功能障碍的细胞并修复受损的组织。干细胞移植可直接促进伤口局部细胞创伤修复, 成为干细胞促进皮肤创伤愈合的重要途径。
2 、胚胎干细胞移植
胚胎干细胞 (embryonic stem cells, ESCs) 是来源于哺乳动物早期胚胎细胞团中的二倍体细胞, 体外培养后, 胚胎干细胞仍具有稳定分化成各胚层的潜能。如可通过添加特异的诱导因子或抑制分化因子, 促使胚胎干细胞分化成皮肤组织的多种类型细胞而用于皮肤创伤改善。在糖尿病伤口愈合早期阶段, 干细胞移植可通过增加表皮生长因子、血管内皮生长因子和纤连蛋白的表达量,促进表皮细胞再生, 肉芽组织形成, 血管新生以及成纤维细胞的增殖。从而纠正由于以上功能不足而导致的糖尿病伤口愈合障碍的病理性缺陷。
3、成体干细胞移植
成体干细胞 (adult stem cells, ASCs) 是指存在于已分化组织中的未分化细胞。这种细胞能够自我更新并且能够分化形成相应类型组织的细胞。成体干细胞存在于机体的各种组织器官中, 在病理状态或外因诱导下可以表现出不同程度的再生及自我更新能力。自身成体干细胞移植在应用时不存在组织相容性问题, 理论上可以避免移植排斥反应和免疫抑制剂的使用。成体干细胞致瘤风险低, 伦理学争议少。因此, 成体干细胞已成为当前临床应用的理想选择。
3.1 骨髓间充质干细胞
骨髓间充质干细胞 (bone marrow-derived mesenchymal stem cells, BM-MSCs), 也称间质祖细胞, 可以分化为多种不同类型的细胞, 如脂肪细胞和成纤维细胞等。
研究发现, 不仅从真皮中分离培养的干细胞可以促进皮肤伤口愈合, 骨髓间充质干细胞也可以促进皮肤难愈性创面的愈合,移植的骨髓间充质干细胞可以在皮肤内分化成角蛋白细胞、上皮细胞和内皮细胞[2], 并且促进表皮细胞再生, 细胞重塑以及血管新生, 伤口处的骨髓间充质干细胞可表达 CD34+ 、形成特有的角化细胞并分泌角质蛋白促进腺体的形成, 同时, 培养过骨髓间充质干细胞的培养液也可以促进上皮细胞管腔结构的形成。以上研究表明骨髓间充质干细胞可通过分化和释放促血管生成因子而促进伤口愈合。
3.2 脂肪来源干细胞
脂肪来源干细胞 (adiposederived stem cells, ADSCs) 是多潜能干细胞, 能够分化成多种细胞, 并可分泌血管生长因子, 为治愈糖尿病伤口带来了新希望, 在伤口愈合和组织修复方面具有巨大应用前景,脂肪干细胞可自发地分化成上皮细胞和内皮细胞, 并能分泌促血管生成的生长因子, 如血管内皮生长因子、肝细胞生长因子和成纤维生长因子, 进而增加血管生成, 增强伤口愈合能力, 加速伤口愈合。
3.3 脐带血干细胞
脐血干细胞 (umbilical cord derived stem cells, UC-DSCs) 具有与骨髓干细胞相似的特性。 Romanov 等发现嵴髓血管中含有大量类似于间充质干细胞样的细胞, 这些细胞可形成成纤维细胞集落并可成功在体外扩增培养。Shrestha 等将来源于脐带的间充质干细胞移植到糖尿病小鼠伤口周围, 发现其可通过促进表皮细胞再生、旁分泌因子的分泌和血管新生等途径促进糖尿病小鼠伤口愈合。同时也有研究表明, 来源于脐带血的干细胞在体外条件下可以被分化成上皮细胞而应用于有缺陷的皮肤表层。

3.4皮肤干细胞
研究发现, 分离出的皮肤干细胞 (cutaneous stem cells, CSCs) 具有巨大的应用潜能。毛发滤泡具有自我更新能力, 成为一种新兴的多潜能干细胞的代表。Roh 等[60]报道, 人的毛囊隆突区来源的毛囊干细胞可分化为上皮和分泌脂质细胞。这类干细胞更易进入皮肤组织, 相信这将成为新兴的治愈皮肤伤口的有效方法。
干细胞改善皮肤愈合未来展望
干细胞改善伤口愈合已经从一个纯粹的科学实验研究慢慢转向临床应用研究。目前研究已初步阐明干细胞增殖和分化的机制, 证明其在细胞改善学发展中的本质, 并说明不同的干细胞在体内和体外的可塑性以及未来在临床方面的应用。然而, 在干细胞促进伤口愈合方面仍需面临一些问题, 如最佳靶细胞的选择、连续改善方法的选取、机体的免疫排斥等。因此, 只有深入研究干细胞具有多能性的分子机制及其特有的分化途径, 才能将其更好地应用于疾病的改善中。随着干细胞理论的日臻完善和研究技术的迅勐发展, 相信干细胞疗法必将在疾病改善和生物医药等领域取得划时代的成果。
推荐阅读:干细胞治疗:干细胞治疗方式及分类
本文链接地址:http://www.domo-kenkou.com/gxbzs/tnb/2121.html